DREPANOCYTOSE
Qu’est-ce que c’est ?
Crédits photo: AFP
La drépanocytose, aussi appelée anémie falciforme, est une maladie chronique, génétique et héréditaire causée par une mutation sur le chromosome 11. Elle est caractérisée par une anomalie de l’hémoglobine, principale protéine du globule rouge ou hématie. Les globules rouges des drépanocytaires ont tendance, surtout en cas d’hypoxie, à former des polymères qui déforment les globules rouges ( forme S ou en faucille) et qui s’agglutinent entres elles, perturbent la circulation sanguine, causent des crises vaso-occlusives extrêmement douloureuses et favorisent les infections. La différence entre l’hémoglobine S et l’hémoglobine de type normale A est que l’hémoglobine normale est soluble quand elle a de l’oxygène, et elle est aussi soluble quand elle n’en a pas.
L’hémoglobine transporte l’oxygène depuis les poumons vers les tissus et participe à l’élimination du dioxyde de carbone. Dans la drépanocytose, la forme anormale adoptée par l’hématie les rend fragiles et rigides. La rate ne les reconnaît pas donc elle les détruit. Ces anomalies favorisent donc l’anémie. De plus, des micro-caillots se forment et peuvent devenir de plus en plus gros et la véritable létalité de la drépanocytose n’est donc pas due à l’anémie, mais à cette maladie vasculaire. Environ un tiers des personnes homozygotes pour l’hémoglobine S ont un ou plusieurs AVC avant l’âge de 10 ans. Et chez les quelques chanceux qui parviennent à atteindre l’âge de l’adolescence, ces caillots peuvent s’accumuler dans les poumons et provoquer une maladie très grave appelée syndrome thoracique aigu, qui est essentiellement de l’emphysème ou la destruction des poumons par ces obstructions. Environ un tiers des patients vivront en bonne santé jusqu’à l’âge adulte, mais ils ont de nombreux problèmes de santé et leur durée de vie est considérée comme plus courte. Elle est aujourd’hui de plus de 40 ans alors qu’elle était inférieure à 20 ans avant les années 1980. Cependant, il reste encore beaucoup à faire pour améliorer le quotidien et l’espérance de vie des malades.
Mode de transmission
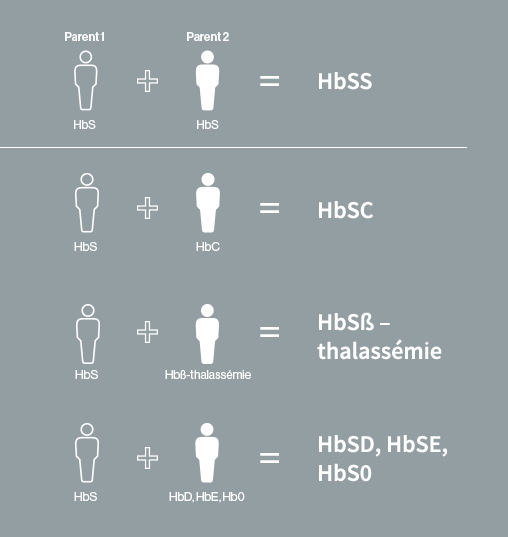
La maladie est transmise selon un mode de transmission dite autosomique récessive : chacun des parents doit transmettre le gène muté à l’enfant pour que la maladie se déclare chez ce dernier.
Il existe plusieurs types de drépanocytose. La forme la plus fréquente, responsable des cas les plus graves, est associée à la présence de deux copies du gène de l’hémoglobine S, une sur chaque chromosomes 11 (forme homozygote SS). Dans les autres formes de la maladie, les patients ne sont porteurs que d’une seule copie du gène codant pour l’hémoglobine S, la seconde copie porte une mutation différente soit C, ce qui conduit à la forme double hétérozygote SC par exemple ou d’autres comme les thalassémies -(voir schéma)
Origine
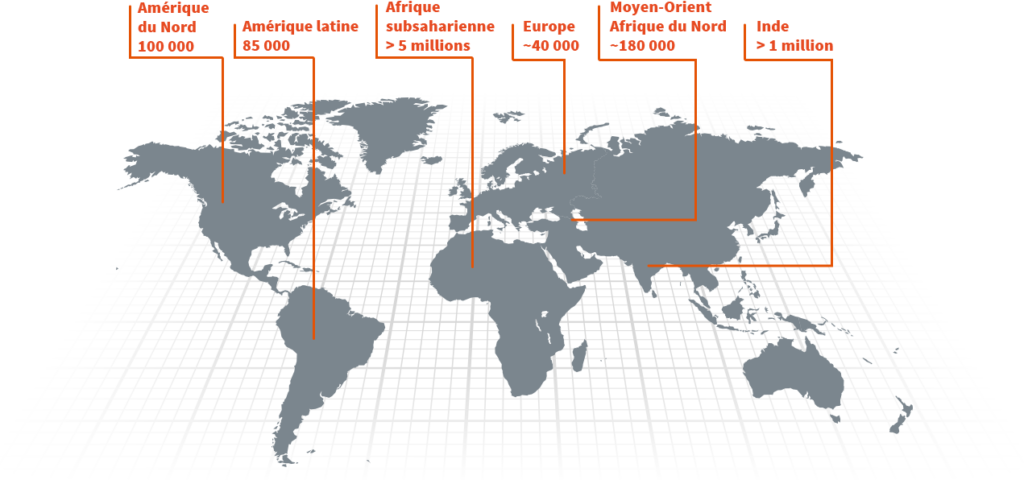
Étant originaire d’Afrique, elle touche principalement les personnes d’ascendance africaine. La mutation aurait été «motivée» par une réaction génétique en vue de protéger contre le paludisme qui sévissait dans certaines zones. Il a ainsi été établi que le trait drépanocytaire protégeait contre le paludisme. A la suite des migrations et métissages, ce gène est sorti de «sa zone de confort» et il s’est depuis répandue au point de devenir la maladie génétique la plus répandue dans le monde. La drépanocytose est très présente en Inde, en Amérique, tout particulièrement aux États-Unis, Antilles et au Brésil, ainsi qu’en Europe de l’Ouest. Par conséquent, les personnes d’ascendance méditerranéenne, moyen-orientale, caucasienne, indienne, hispanique, native américaine, entre autres, peuvent également être touchées.
Carte Insérer l’infographie
Globule rouge d’un malade atteint de drépanocytose (ou anémie à cellules falciformes). L’origine de la drépanocytose provient de la modification d’un seul acide aminé, ce qui entraîne une perte d’élasticité membranaire et produit des hémolyses. © Inserm, C. Féo
L’hémoglobine des sujets drépanocytaires est dite « hémoglobine S », pour Sickle qui veut dire faucille en anglais.
Des symptômes très variables et souvent imprévisibles
Les symptômes de la maladie sont variables et dépendent non seulement de l’âge, mais aussi de la sévérité de la drépanocytose.
Dans les tous premiers mois, les nourrissons sont généralement asymptomatiques car ils bénéficient de la présence d’hémoglobine fœtale, la forme d’hémoglobine produite chez le fœtus durant la période in utero, qui n’est pas mutée quant à elle. Elle disparaît hélas ensuite, au profit de l’hémoglobine S. Par la suite, les patients ont un risque accru de développer une anémie ou des infections parfois graves (pneumonies, méningites ou septicémies…). Avec l’avancée en âge, ces risques de complications persistent et d’autres apparaissent, plus spécifiques, liés à l’évolution à long terme de la maladie.
L’anémie
L’anémie est souvent le premier signe de la maladie. Elle se traduit par une pâleur et une fatigue chronique, parfois par une jaunisse (ictère).
L’anémie chronique associée à la drépanocytose est causée par les polymères d’hémoglobine S qui fragilisent les globules rouges et favorisent leur destruction précoce (hémolyse). Alors que la durée de vie moyenne des hématies est normalement de 120 jours, elle tombe à une vingtaine de jours seulement chez les personnes atteintes de drépanocytose.
L’anémie est susceptible de s’aggraver brutalement en cas de suractivité de la rate dans la destruction des globules rouges anormaux. On parle alors de séquestration splénique aiguë.
Les crises vaso-occlusives
Les crises dites « vaso-occlusives » sont déclenchées par les globules rouges rigidifiés par les polymères d’hémoglobine S, qui obstruent la circulation sanguine dans les petits vaisseaux sanguins. Ces crises entraînent des douleurs aiguës souvent extrêmement violentes et affectent les os, les articulations des bras et des jambes, le dos ou la poitrine. Chez les tout petits, la crise se manifeste généralement par un gonflement douloureux des mains et des pieds (syndrome pied-main).
Les occlusions vasculaires associées à la drépanocytose peuvent être à l’origine de complications majeures. Ainsi, le syndrome thoracique aigu constitue une complication fréquente dans les jours suivant l’installation d’une crise vaso-occlusive. Il correspond même à la première cause de décès des patients atteints de drépanocytose. Dans ce cas, la vaso-occlusion affecte le poumon et compromet l’oxygénation de tout l’organisme. Cela se traduit par des difficultés respiratoires et des douleurs dans la poitrine, parfois accompagnées d’une fièvre.
Les accidents vasculaires cérébraux (AVC) sont également communs chez les drépanocytaires, surtout chez les enfants. Enfin, la répétition des vaso-occlusions peut aboutir à la nécrose de certains tissus comme l’os (ostéonécrose de la tête fémorale) ou d’organes. Par ailleurs très sollicitée pour assurer l’hémolyse des hématies falciformes, la rate des patients drépanocytaires fait ainsi partie des organes précocement lésée par les vaso-occlusions. Elle n’assure alors plus complètement son rôle, ce qui peut favoriser la survenue d’infections bactériennes.
La sensibilité aux infections
Les infections exacerbent les autres manifestations de la drépanocytose comme l’anémie et les occlusions vasculaires. D’autre part, elles représentent toujours un risque de mortalité (septicémie foudroyante), tout particulièrement chez les enfants aux mécanismes de défense affaiblis.
Complications à long terme
Au fil des ans, toutes ces manifestations de la maladie mettent l’organisme à rude épreuve. Elles sont susceptibles de toucher presque tous les organes notamment le rein (insuffisance rénale), le système ostéo-articulaire (arthrose, ostéoporose), l’œil (hémorragies intraoculaires), le foie, les poumons (hypertension artérielle pulmonaire) ou encore la vésicule biliaire (calculs).
Un diagnostic aussi précoce que possible
Ce diagnostic est réalisé en premier lieu à partir d’un simple échantillon de sang analysé par différentes méthodes (électrophorèse, isoélectrofocalisation ou chromatographie) aptes à distinguer l’hémoglobine S de l’hémoglobine normale A et des autres variants de l’hémoglobine, sur la base de leurs différences physico-chimiques. Les progrès dans la prise en charge de la maladie ont permis d’accroître significativement l’espérance de vie moyenne des personnes atteintes de drépanocytose.
Le dépistage néonatal
La France déploie un dépistage néonatal systématique chez tous les enfants nés de parents issus des populations les plus concernées par la maladie. Il est réalisé à la maternité à la 72ème heure de vie du nourrisson (dans le cadre plus large du dépistage des maladies rares), à partir d’un échantillon sanguin prélevé au niveau du talon du nouveau-né.
Une prévention active et des traitements symptomatiques
Pour la plupart des patients, la prise en charge de la drépanocytose s’articule autour d’une prévention des complications et d’un suivi médical régulier. Le dépistage néonatal constitue un outil indispensable.
La prévention des complications
La prophylaxie du risque infectieux consiste à administrer préventivement des antibiotiques et à renforcer le programme vaccinal, tout particulièrement chez les nourrissons et les jeunes enfants. Un supplément en acide folique et en fer est aussi prescrit pour renforcer la production des globules rouges et prévenir l’anémie.
Une bonne hygiène de vie
Ces bonnes habitudes vont consister en :
- Adopter une alimentation équilibrée.
- Bonne hydratation est nécessaire ( boire beaucoup d’eau)
- Eviter l’exposition à des températures extrêmes ou à des variations importantes de température.
- Eviter les efforts trop intenses liés à la pratique de sports extrêmes et d’endurance sont à proscrire.
- Eviter les pièces mal aérées et les séjours à plus de 1 500 mètres d’altitude où l’oxygène se raréfie ( hypoxie).
- Porter des vêtements amples ne coupant pas la circulation sanguine.
- Avoir suivi médical régulier permet d’évaluer l’évolution de la maladie et les dégâts qu’elle cause sur les organes.
- Suivre particulièrement les fonctions rénale et respiratoire ainsi que l’état de l’œil. Une échographie cérébrale (Doppler transcrânien) est régulièrement réalisée pour prévenir un risque d’AVC.
Les transfusions sanguines
La transfusion sanguine est un outil important dans la prise en charge des patients drépanocytaires. Elle consiste à transfuser le malade avec le sang d’un donneur sain compatible, permettant ainsi de rétablir un taux acceptable de globules rouges en cas d’anémie aggravée et de « diluer » les globules rouges falciformes avec des globules rouges normaux.
Cependant, les transfusions répétées peuvent entraîner une alloimmunisation érythrocytaire : le système immunitaire du malade se met à réagir contre le sang du donneur, considéré comme étranger.
La prise en charge des crises douloureuses
En cas de crise vaso-occlusive, les antalgiques soulagent la douleur. Si la douleur persiste, une hospitalisation est nécessaire. La force des antalgiques sera alors augmentée jusqu’à l’administration de morphine ou de dérivés opioïdes pour les douleurs les plus résistantes. La prise d’antalgiques est parfois complétée par une oxygénothérapie.
Pour diminuer l’occurrence de crises douloureuses, l’hydroxycarbamide (ou hydroxyurée) peut être prescrite. Ce médicament agit à plusieurs niveaux dans la prévention des vaso-occlusions. Il permet notamment d’augmenter la production de l’hémoglobine fœtale, exempte de mutation et présente en faible concentration chez l’adulte, et réduit la polymérisation de l’hémoglobine S. Ce traitement a permis de grandement améliorer la qualité de vie des patients drépanocytaires. Cependant son efficacité peut diminuer avec l’âge et tous les adultes n’y répondent pas. Par ailleurs, l’hydroxycarbamide peut conduire à des problèmes (réversibles) de fertilité chez les hommes.
La greffe de moelle osseuse
Le seul traitement curatif actuellement disponible contre la drépanocytose est la greffe de moelle osseuse. Cette moelle contient en effet les cellules souches qui donnent naissance aux cellules sanguines, dont les globules rouges. Concrètement, les cellules souches de la moelle du patient sont détruites et remplacées par celles d’un donneur sain compatible, souvent un frère ou une sœur. Cette procédure offre plus de 95% de succès et il est possible de trouver un donneur compatible dans 70% des cas. Elle reste néanmoins très lourde et coûteuse. Elle est donc réservée aux formes les plus sévères de la maladie, notamment chez l’enfant. En France, une vingtaine de patients bénéficient d’une telle greffe chaque année.
Une recherche sans frontière
La recherche sur la drépanocytose s’appuie beaucoup sur des collaborations avec les régions les plus affectées par la maladie. Les chercheurs s’attachent en outre à développer des coopérations avec les pays à faible revenu où se concentre la plupart des patients drépanocytaires. Mieux comprendre la maladie et sa physiopathologie au travers de l’épidémiologie des complications cardio-vasculaires, tel est par exemple l’objectif du projet CADRE développé par des chercheurs de l’INSERM ( Brigitte Ranque et Xavier Jouven) et GR-Ex laboratoire d’excellence sur la globule rouge dans plusieurs pays d’Afrique (Cameroun, Sénégal, Mali, Côte d’Ivoire et République Démocratique du Congo), il y a d’autres exemple…
De nombreuses personnes sont touchées par la drépanocytose si les traitements actuels ont permis d’augmenter grandement l’espérance de vie des patients affectés, ils restent encore limités. La prise en charge de la douleur lors des crises reste une vraie problématique pour les patients. La recherche poursuit donc ses efforts pour améliorer la qualité de vie, voire traiter la maladie à la source, là où naissent les globules rouges.
Des pistes ouvertes grâce à la génétique et l’épigénétique
Les espoirs de la thérapie génique
De part la lourdeur des greffes de moelle osseuse et la difficulté à trouver des donneurs compatibles, les perspectives de guérison de la drépanocytose reposent plus volontiers sur la thérapie génique. Cette approche vise à « greffer » un gène sain de la bêta-globine dans les cellules souches hématopoïétiques des malades drépanocytaires.
Globule rouge d’un malade atteint de drépanocytose (ou anémie à cellules falciformes). L’origine de la drépanocytose provient de la modification d’un seul acide aminé, ce qui entraîne une perte d’élasticité membranaire et produit des hémolyses. © Inserm, C. Féo
L’hémoglobine des sujets drépanocytaires est dite « hémoglobine S », pour Sickle qui veut dire faucille en anglais.
Des symptômes très variables et souvent imprévisibles
Les symptômes de la maladie sont variables et dépendent non seulement de l’âge, mais aussi de la sévérité de la drépanocytose.
Dans les tous premiers mois, les nourrissons sont généralement asymptomatiques car ils bénéficient de la présence d’hémoglobine fœtale, la forme d’hémoglobine produite chez le fœtus durant la période in utero, qui n’est pas mutée quant à elle. Elle disparaît hélas ensuite, au profit de l’hémoglobine S. Par la suite, les patients ont un risque accru de développer une anémie ou des infections parfois graves (pneumonies, méningites ou septicémies…). Avec l’avancée en âge, ces risques de complications persistent et d’autres apparaissent, plus spécifiques, liés à l’évolution à long terme de la maladie.
L’anémie
L’anémie est souvent le premier signe de la maladie. Elle se traduit par une pâleur et une fatigue chronique, parfois par une jaunisse (ictère).
L’anémie chronique associée à la drépanocytose est causée par les polymères d’hémoglobine S qui fragilisent les globules rouges et favorisent leur destruction précoce (hémolyse). Alors que la durée de vie moyenne des hématies est normalement de 120 jours, elle tombe à une vingtaine de jours seulement chez les personnes atteintes de drépanocytose.
L’anémie est susceptible de s’aggraver brutalement en cas de suractivité de la rate dans la destruction des globules rouges anormaux. On parle alors de séquestration splénique aiguë.
Les crises vaso-occlusives
Les crises dites « vaso-occlusives » sont déclenchées par les globules rouges rigidifiés par les polymères d’hémoglobine S, qui obstruent la circulation sanguine dans les petits vaisseaux sanguins. Ces crises entraînent des douleurs aiguës souvent extrêmement violentes et affectent les os, les articulations des bras et des jambes, le dos ou la poitrine. Chez les tout petits, la crise se manifeste généralement par un gonflement douloureux des mains et des pieds (syndrome pied-main).
Les occlusions vasculaires associées à la drépanocytose peuvent être à l’origine de complications majeures. Ainsi, le syndrome thoracique aigu constitue une complication fréquente dans les jours suivant l’installation d’une crise vaso-occlusive. Il correspond même à la première cause de décès des patients atteints de drépanocytose. Dans ce cas, la vaso-occlusion affecte le poumon et compromet l’oxygénation de tout l’organisme. Cela se traduit par des difficultés respiratoires et des douleurs dans la poitrine, parfois accompagnées d’une fièvre.
Les accidents vasculaires cérébraux (AVC) sont également communs chez les drépanocytaires, surtout chez les enfants. Enfin, la répétition des vaso-occlusions peut aboutir à la nécrose de certains tissus comme l’os (ostéonécrose de la tête fémorale) ou d’organes. Par ailleurs très sollicitée pour assurer l’hémolyse des hématies falciformes, la rate des patients drépanocytaires fait ainsi partie des organes précocement lésée par les vaso-occlusions. Elle n’assure alors plus complètement son rôle, ce qui peut favoriser la survenue d’infections bactériennes.
La sensibilité aux infections
Les infections exacerbent les autres manifestations de la drépanocytose comme l’anémie et les occlusions vasculaires. D’autre part, elles représentent toujours un risque de mortalité (septicémie foudroyante), tout particulièrement chez les enfants aux mécanismes de défense affaiblis.
Complications à long terme
Au fil des ans, toutes ces manifestations de la maladie mettent l’organisme à rude épreuve. Elles sont susceptibles de toucher presque tous les organes notamment le rein (insuffisance rénale), le système ostéo-articulaire (arthrose, ostéoporose), l’œil (hémorragies intraoculaires), le foie, les poumons (hypertension artérielle pulmonaire) ou encore la vésicule biliaire (calculs).
Un diagnostic aussi précoce que possible
Ce diagnostic est réalisé en premier lieu à partir d’un simple échantillon de sang analysé par différentes méthodes (électrophorèse, isoélectrofocalisation ou chromatographie) aptes à distinguer l’hémoglobine S de l’hémoglobine normale A et des autres variants de l’hémoglobine, sur la base de leurs différences physico-chimiques. Les progrès dans la prise en charge de la maladie ont permis d’accroître significativement l’espérance de vie moyenne des personnes atteintes de drépanocytose.
Le dépistage néonatal
La France déploie un dépistage néonatal systématique chez tous les enfants nés de parents issus des populations les plus concernées par la maladie. Il est réalisé à la maternité à la 72ème heure de vie du nourrisson (dans le cadre plus large du dépistage des maladies rares), à partir d’un échantillon sanguin prélevé au niveau du talon du nouveau-né.
Une prévention active et des traitements symptomatiques
Pour la plupart des patients, la prise en charge de la drépanocytose s’articule autour d’une prévention des complications et d’un suivi médical régulier. Le dépistage néonatal constitue un outil indispensable.
La prévention des complications
La prophylaxie du risque infectieux consiste à administrer préventivement des antibiotiques et à renforcer le programme vaccinal, tout particulièrement chez les nourrissons et les jeunes enfants. Un supplément en acide folique et en fer est aussi prescrit pour renforcer la production des globules rouges et prévenir l’anémie.
Une bonne hygiène de vie
Ces bonnes habitudes vont consister en :
- Adopter une alimentation équilibrée.
- Bonne hydratation est nécessaire ( boire beaucoup d’eau)
- Eviter l’exposition à des températures extrêmes ou à des variations importantes de température.
- Eviter les efforts trop intenses liés à la pratique de sports extrêmes et d’endurance sont à proscrire.
- Eviter les pièces mal aérées et les séjours à plus de 1 500 mètres d’altitude où l’oxygène se raréfie ( hypoxie).
- Porter des vêtements amples ne coupant pas la circulation sanguine.
- Avoir suivi médical régulier permet d’évaluer l’évolution de la maladie et les dégâts qu’elle cause sur les organes.
- Suivre particulièrement les fonctions rénale et respiratoire ainsi que l’état de l’œil. Une échographie cérébrale (Doppler transcrânien) est régulièrement réalisée pour prévenir un risque d’AVC.
Les transfusions sanguines
La transfusion sanguine est un outil important dans la prise en charge des patients drépanocytaires. Elle consiste à transfuser le malade avec le sang d’un donneur sain compatible, permettant ainsi de rétablir un taux acceptable de globules rouges en cas d’anémie aggravée et de « diluer » les globules rouges falciformes avec des globules rouges normaux.
Cependant, les transfusions répétées peuvent entraîner une alloimmunisation érythrocytaire : le système immunitaire du malade se met à réagir contre le sang du donneur, considéré comme étranger.
La prise en charge des crises douloureuses
En cas de crise vaso-occlusive, les antalgiques soulagent la douleur. Si la douleur persiste, une hospitalisation est nécessaire. La force des antalgiques sera alors augmentée jusqu’à l’administration de morphine ou de dérivés opioïdes pour les douleurs les plus résistantes. La prise d’antalgiques est parfois complétée par une oxygénothérapie.
Pour diminuer l’occurrence de crises douloureuses, l’hydroxycarbamide (ou hydroxyurée) peut être prescrite. Ce médicament agit à plusieurs niveaux dans la prévention des vaso-occlusions. Il permet notamment d’augmenter la production de l’hémoglobine fœtale, exempte de mutation et présente en faible concentration chez l’adulte, et réduit la polymérisation de l’hémoglobine S. Ce traitement a permis de grandement améliorer la qualité de vie des patients drépanocytaires. Cependant son efficacité peut diminuer avec l’âge et tous les adultes n’y répondent pas. Par ailleurs, l’hydroxycarbamide peut conduire à des problèmes (réversibles) de fertilité chez les hommes.
La greffe de moelle osseuse
Le seul traitement curatif actuellement disponible contre la drépanocytose est la greffe de moelle osseuse. Cette moelle contient en effet les cellules souches qui donnent naissance aux cellules sanguines, dont les globules rouges. Concrètement, les cellules souches de la moelle du patient sont détruites et remplacées par celles d’un donneur sain compatible, souvent un frère ou une sœur. Cette procédure offre plus de 95% de succès et il est possible de trouver un donneur compatible dans 70% des cas. Elle reste néanmoins très lourde et coûteuse. Elle est donc réservée aux formes les plus sévères de la maladie, notamment chez l’enfant. En France, une vingtaine de patients bénéficient d’une telle greffe chaque année.
Une recherche sans frontière
La recherche sur la drépanocytose s’appuie beaucoup sur des collaborations avec les régions les plus affectées par la maladie. Les chercheurs s’attachent en outre à développer des coopérations avec les pays à faible revenu où se concentre la plupart des patients drépanocytaires. Mieux comprendre la maladie et sa physiopathologie au travers de l’épidémiologie des complications cardio-vasculaires, tel est par exemple l’objectif du projet CADRE développé par des chercheurs de l’INSERM ( Brigitte Ranque et Xavier Jouven) et GR-Ex laboratoire d’excellence sur la globule rouge dans plusieurs pays d’Afrique (Cameroun, Sénégal, Mali, Côte d’Ivoire et République Démocratique du Congo), il y a d’autres exemple…
De nombreuses personnes sont touchées par la drépanocytose si les traitements actuels ont permis d’augmenter grandement l’espérance de vie des patients affectés, ils restent encore limités. La prise en charge de la douleur lors des crises reste une vraie problématique pour les patients. La recherche poursuit donc ses efforts pour améliorer la qualité de vie, voire traiter la maladie à la source, là où naissent les globules rouges.
Des pistes ouvertes grâce à la génétique et l’épigénétique
Les espoirs de la thérapie génique
De part la lourdeur des greffes de moelle osseuse et la difficulté à trouver des donneurs compatibles, les perspectives de guérison de la drépanocytose reposent plus volontiers sur la thérapie génique. Cette approche vise à « greffer » un gène sain de la bêta-globine dans les cellules souches hématopoïétiques des malades drépanocytaires.
Sources:
https://www.inserm.fr/dossier/drepanocytose/
https://robertdebre.aphp.fr/drepanocytose/
https://www.notaloneinsicklecell.com/fr/Global-Impact-Of-SCD/
https://www.genome.gov/genetics-glossary/Sickle-Cell-Disease
https://www.sparksicklecellchange.com
https://www.rarediseaseadvisor.com
La drépanocytose en Afrique : les défis d’une meilleure prise en charge pour les millions de personnes atteintes – BBC News Afrique
www.notaloneinsicklecell.com
L’impact mondial de la drépanocytose | NotAloneInSickleCell.com